Sem aprovação da Anvisa, primeiro lote da Sputnik V produzido no Brasil será exportado
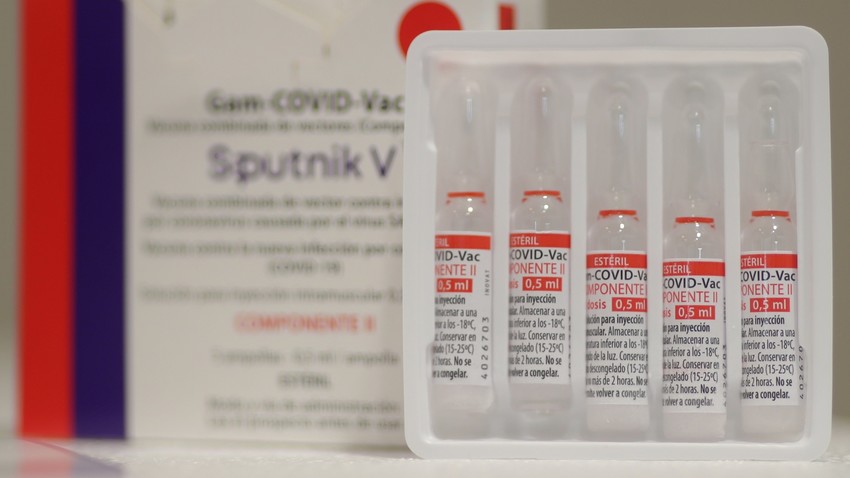
Frascos contendo vacinas Sputnik V feitos com ingredientes e tecnologia fornecidos pela Rússia são fotografados nas instalações da farmacêutica União Química, em Guarulhos
ReutersO Centro Gamaleya de Moscou, que desenvolveu a vacina Sputnik V, anunciou nesta quinta-feira (20) a produção do primeiro lote comercial do imunizante russo na fábrica da União Química, no Brasil. O anúncio foi feito por meio do canal do instituto no Telegram.
“O primeiro lote da Sputnik V foi produzido no Brasil. A líder farmacêutica brasileira União Química lançou um lote do medicamento russo”, diz a publicação.
O Centro Gamaleya supervisionou o controle de qualidade da vacina que foi envasada na fábrica da União Química em Guarulhos, na região metropolitana de São Paulo.
A expectativa agora é que o imunizante seja exportado para outros países da América Latina, uma vez que seu uso emergencial em território brasileiro ainda não foi autorizado pela Anvisa.
A União Química não especificou quantas doses foram produzidas nem para quais países a Sputnik V produzida no Brasil será enviada. Sabe-se, porém, que o primeiro lote com 100 mil doses foi embalado em caixas com rótulo em espanhol. Países como Paraguai, Uruguai e Argentina também já teriam mostrado interesse em adquirir o lote.
Segundo o executivo-chefe da farmacêutica, Fernando Marques, a fábrica será capaz de produzir até 8 milhões de doses ao mês quando a Anvisa aprovar o uso da Sputnik V no Brasil.
Sem prazo para liberação no Brasil
No último dia 26 de março, a Anvisa proibiu a importação e uso da vacina russa Sputnik V no país, após decisão aprovada por unanimidade pelos membros do conselho diretivo. Segundo os técnicos brasileiros, além da ausência de informações importantes para a análise do pedido de uso emergencial, os dados recebidos e a visita a instalações de produção na Rússia dariam margem a dúvidas sobre aspectos do imunizante e seus respectivos estudos.
Após as declarações da diretoria da Anvisa, o Instituto Gamaleya divulgou uma nota para esclarecer o que chamou de “campanha de desinformação contra a Sputnik V”.
“Comentários recentes imprecisos e enganosos do regulador brasileiro Anvisa alegaram detecção de adenovírus replicado (RCA), uma partícula viral enfraquecida que nem mesmo causa um resfriado comum, na Sputnik V (...) O Instituto Gamaleya confirma que nenhum RCA foi detectado em nenhum dos lotes da vacina Sputnik V”, lê-se no comunicado.
Em meio a polêmica, os ministérios da Saúde e das Relações Exteriores do Brasil divulgaram uma nota à imprensa reforçando o apoio à continuidade do “o diálogo em curso, sempre respeitando a autonomia da Anvisa, de modo que a Sputnik V, no momento em que seu uso for aprovado no Brasil, venha a reforçar o programa nacional de imunização contra a covid-19”.
O porta-voz do Kremlin, Dmítri Peskov, também garantiu que a Rússia continuará a manter contatos sobre a vacina com o Brasil, destacando que “se o lado brasileiro não tiver dados, eles serão fornecidos”.
A Sputnik V, desenvolvida por especialistas do Centro Gamaleya, foi registrada em agosto do ano passado e se tornou a primeira vacina contra o coronavírus na Rússia e no mundo. O imunizante, já aprovado em 66 países, está entre as três principais vacinas contra covid do mundo em termos de número de aprovações recebidas por agências governamentais.
LEIA TAMBÉM: Equador planeja importação de vacina russa contra covid-19
Autorizamos a reprodução de todos os nossos textos sob a condição de que se publique juntamente o link ativo para o original do Russia Beyond.
Assine
a nossa newsletter!
Receba em seu e-mail as principais notícias da Rússia na newsletter: