Anvisa solicita mais dados sobre vacina russa Sputnik V e decisão sobre uso emergencial é adiada
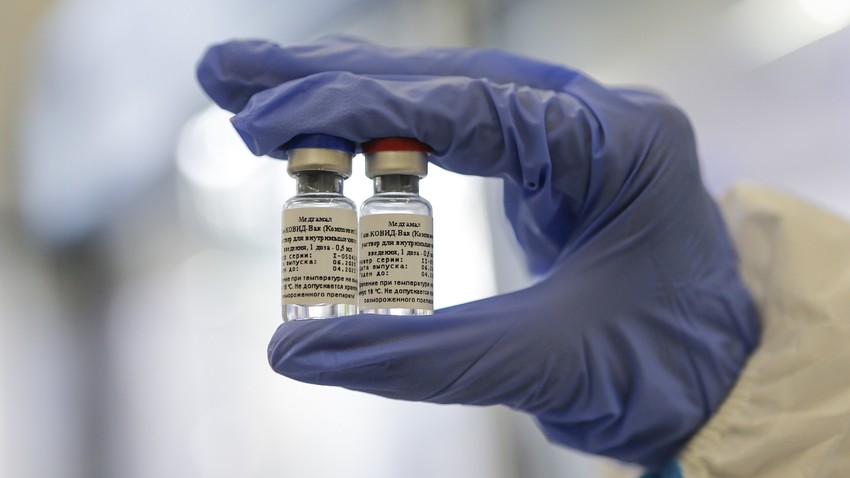
A Anvisa (Agência Nacional de Vigilância Sanitária) solicitou o envio de novos dados sobre a vacina russa contra o coronavírus, Sputnik V, antes de considerar sua aprovação para uso emergencial no Brasil. De acordo com a agência, a solicitação não atende aos critérios mínimos para aprovação imediata, o que não significaria a recusa de uma aprovação futura.
“O pedido foi devolvido à União Química, por não cumprir os critérios mínimos – nomeadamente, por falta de autorização para a terceira fase dos ensaios clínicos, bem como no que diz respeito à questão dos métodos avançados de produção”, lê-se no site da Anvisa.
No final de dezembro passado, a União Química solicitou à Anvisa autorização para conduzir a fase 3 dos ensaios clínicos da vacina Sputnik V no Brasil. A agência informou que resolveria em 72 horas, porém, mais tarde, solicitou mais informações sobre o imunizante.
Na última sexta (15), a União Química e o Fundo Russo de Investimento Direto (RDIF), que financiou o desenvolvimento da Sputnik V, entraram com um pedido de uso emergencial de 10 milhões de doses da vacina russa no Brasil.
“A União Química acredita que, em resposta à escalada da pandemia no Brasil e no mundo, o Estado e as empresas devem fazer todos os esforços para combatê-la, inclusive tomar medidas de caráter emergencial e excepcional, justificadas pela necessidade urgente e a importância do momento atual”, afirmou um representante da empresa na ocasião.
O acordo acertado entre as partes na última quinta-feira (14), em Moscou, pressupõe a entrega de 10 milhões de doses da Sputnik V ao Brasil no primeiro trimestre de 2021. As primeiras doses deveriam chegar em janeiro.
No início deste ano, a União Química recebeu material celular para produção da vacina, que supostamente começaria na sexta passada.
“Procedimento padrão”, diz Fundo russo
O Fundo Russo de Investimento Direto (RDIF) refutou as notícias de que o Brasil teria se “recusado a acelerar o registro” da vacina contra o coronavírus Sputnik V, destacando que a Anvisa apenas solicitou mais informações sobre o imunizante.
“Em meio a informações falsas em algumas reportagens na imprensa sobre a recusa do registro acelerado da vacina Sputnik V no Brasil, informamos que a Agência Nacional de Vigilância Sanitária (Anvisa) solicitou informações adicionais sobre a vacina Sputnik V, que serão fornecidas em breve”, afirmou o RDIF em um comunicado oficial.
Ainda de acordo com o Fundo, o pedido de informações adicionais pela agência brasileira é “um procedimento padrão e não significa a recusa do registro”.
Neste domingo, (17), a Anvisa declarou que devolvera à União Química os documentos apresentados para aprovação de uso emergencial da vacina russa no Brasil.
Em 11 de agosto de 2020, a Rússia se tornou o primeiro país no mundo a registrar uma vacina contra o coronavírus. A Sputnik V foi desenvolvida pelo Centro Nacional de Pesquisa em Epidemiologia e Microbiologia Gamaleya, do Ministério da Saúde da Rússia.
Outros países da América do Sul, como Argentina, Bolívia e Venezuela, aprovaram o uso emergencial da vacina russa e já iniciaram a vacinação.
LEIA TAMBÉM: Putin ordena que Rússia inicie vacinação em massa na semana que vem
Autorizamos a reprodução de todos os nossos textos sob a condição de que se publique juntamente o link ativo para o original do Russia Beyond.
Assine
a nossa newsletter!
Receba em seu e-mail as principais notícias da Rússia na newsletter: